作者:时代财经 赵鹏宇
一天之内,“神药”瑞德西韦3 项重要临床研究结果同时揭晓,然而结论却令人困惑。
4月30日凌晨,学术期刊《柳叶刀》发布了中日友好医院副院长曹彬和北京协和医学院院校长王辰为通讯作者的一篇论文,报道了在武汉10家医院的237名平均年龄65岁的成人患者中进行的抗病毒药物瑞德西韦的试验结果。
这是该药物的第一项随机双盲对照试验。结果显示,与安慰剂相比,瑞德西韦未能加速新冠疾病重症住院患者的恢复。

图源:视觉中国
然而,另一项备受瞩目的临床研究结论却刚好相反。
当天更早一些,美国吉利德公司官网公布了新冠肺炎潜在治疗药物瑞德西韦(Remdesivir)的一项开放标签的III期SIMPLE新冠肺炎重症患者临床试验结果。在接受5天和10天瑞德西韦治疗的患者中,至少有50%的患者症状有所改善,超过一半的患者在两周内出院。
紧接着,美国国立卫生研究院(NIH)网站发布了一项 1063 名患者的随机对照试验结果,初步数据分析显示,重症患者中瑞德西韦组的康复速度快于安慰剂组。
受上述利好消息影响,吉利德4月29日晚间,股价一度飙涨超10%。截至美股当日收盘,报83.14美元/股,涨5.68%。
图源:雪球
瑞德西韦是美国吉利德科技公司研发的一款抗病毒药物,原计划用于治疗埃博拉出血热和中东呼吸综合征等疾病,尚未在全球任何国家获批上市。
目前,全球范围内 6 项瑞德西韦研究已经有3项公布了结果。但面对大相径庭的研究结论,曹彬教授曾表示,“中国研究和NIH研究不可比较,本质上是两个不同的研究。”
中润医药(集团)有限公司MAH总监、医药研发及并购专家张超4月30日在接受时代财经采访时也表示,“中美分别开展的临床试验设计方案有所不同。从目前披露的临床试验信息分析,在中国开展的临床试验遵循了严格研究方案,受试患者的筛选和纳入标准都更加严格,所得结论更加可靠。”
瑞德西韦对重症无效?
《柳叶刀》最新发表的瑞德西韦在中国进行的临床试验结论并非首次曝光。(点击查看时代财经相关报道:瑞德西韦被曝无效,吉利德大跌概念股受波及)
早在上周,世界卫生组织泄露的数据中就显示,在这项中国研究中,2月6日到3月12日有 237 名新冠肺炎确诊患者参与了该临床试验,其中 158 名患者进入瑞德西韦试验组,79 人在对照组,对于重症患者,接受瑞德西韦的试验组病死率为 13.9%,而接受标准治疗的对照组为 12.8%,两者差异无统计学意义。
当日受此消息影响,资本市场对吉利德的态度急转直下,本来走势良好的股价盘中突然跳水,一度下探超过8%。
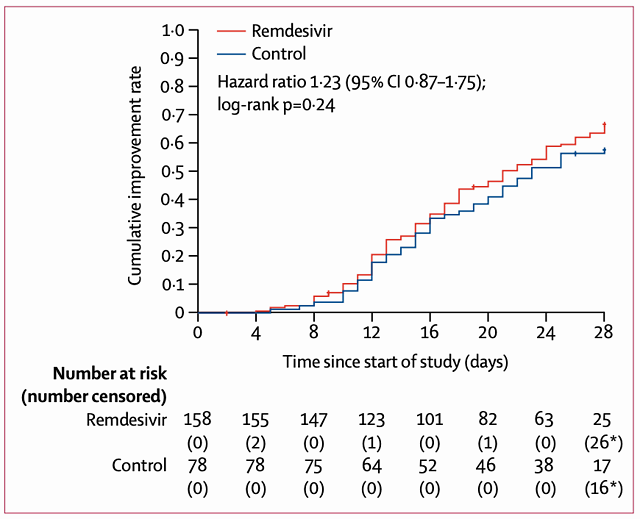
中国试验中,瑞德西韦表现并不显著。(图源:柳叶刀)
曹彬教授在接受媒体采访时表示,“这是一项设计合理的双盲、安慰剂对照、多中心随机试验。项目执行过程非常严格,极少失访。临床试验结果表明,与安慰剂对照组相比,未观察到瑞德西韦可以加快住院患者的病情恢复或降低死亡率。此外,病毒学方面,与安慰剂对照组相比,未观察到瑞德西韦可更快降低上、下呼吸道标本中的病毒载量。”
不过,作者也强调了这项研究的几个局限性:不排除扩大病例数后存在一定治疗效果的可能性;使用了其他的抗病毒药物可能对临床评价构成影响;药物启用时间偏晚,如果能进行早期治疗可能会对减少病毒复制或减缓病情有帮助。
可惜的是,瑞德西韦中国临床试验设计入组重症患者453名,但最终因入组样本数量不足,试验于4月16日提前终止。
爱丁堡大学医学统计学教授、临床研究中心主任约翰诺里(John Norrie)在《柳叶刀》发表的同行评论中也表示,“该试验的双盲、安慰剂对照、多中心、随机的研究设计是很好的,且试验执行情况不错。但试验提前结束,导致研究支持力度不足(underpowered),数据不具有显著的统计学意义,所以无法得出确切的结论。既不能证实瑞德西韦至少能产生一定的临床效果,也无法排除瑞德西韦的有效性。”
一位外企化药研发人员4月30日对时代财经表示,从试验设置方面,更看好曹彬的中国组临床,“比如在发病10天内给药的患者中,接受瑞德西韦的患者似乎比接受安慰剂的患者恢复得更快,平均临床改善时间提到了5天。如果样本量再大一倍的话,可能会达到统计学的意义。但因为试验提前终止数据不能作为参考依据,确实有点可惜了。”
截然相反的临床结论?
就在王辰和曹彬团队上述论文上线前几个小时,在太平洋的另一端,美国方面的研究却出现了截然相反的结论。
根据美国国立卫生研究院(NIH)官网消息,国家过敏症和传染病研究所(NIAID)这项研究结论来自 1063 名患者,是一项随机对照试验研究,也是美国发起的第一项重症患者研究项目。
负责监督试验数据和安全性的独立委员会(DSMB)在 4 月 27 日进行了中期分析。数据表明,相比安慰剂组的患者,瑞德西韦组的患者恢复(指出院或恢复正常活动所需时间)得更快。接受瑞德西韦治疗的患者中位恢复时间为 11 天,而接受安慰剂的患者为 15 天。对于病死率的比较,瑞德西韦组的病死率为 8.0%,而安慰剂组的病死率为 11.6%。
上述化药研发人员向时代财经解释称:“美国这项临床试验结果表明轻型、普通型症状恢复得快,这反映了瑞德西韦这个药物的主要机制,即抑制病毒复制。”
北京解放军302医院感染科临床主任林奕(化名)此前也对时代财经表示,“由于新冠晚期的患者多以炎症风暴为主,瑞德西韦抗病毒的作用并无用武之地,但对于轻症患者抑制病毒方面,瑞德西韦可能会成为一款不错的辅助性用药。”
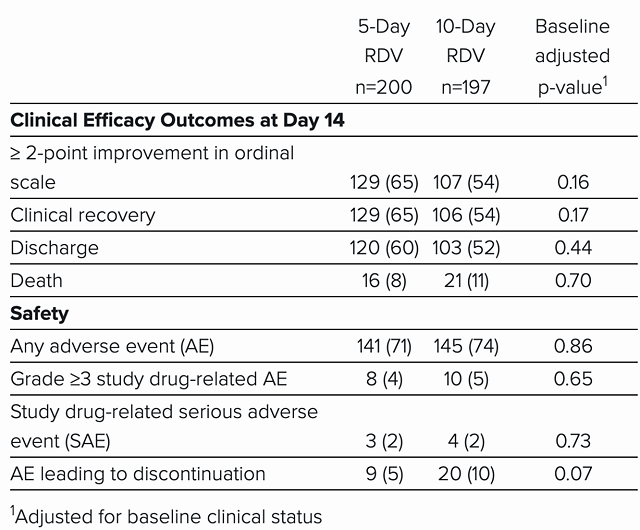
吉利德的研究结论:5 天疗程和 10 天疗程没有明显差异(图源:吉利德)
吉利德公司公布的一项III期SIMPLE新冠肺炎重症患者临床试验也释放了积极信号,不过这项试验并没有设置安慰剂对照组。在业内人士看来,该项研究仅仅是剂量研究,而非药效试验。
张超对时代财经表示,“相较严格的临床试验研究方案,吉利德公司公布的开放标签的SIMPLE试验,无论是纳入标准还是临床试验的观测终点都已经放宽,所得结论自然有所差异。”
张超进一步指出,该项试验结论表明,瑞德西韦有可能缩短病程,但未证明其可以改善病死率。
值得一提的是,该项试验只是吉利德公司SIMPLE试验研究的初步结果。按照计划,该研究将招募 5600 名患者,在全球 180 个试验中心进行研究。
对于吉利德一再扩大瑞德西韦数据样本的行为,张超表示,“吉利德公司寄希望于开展多组临床试验,通过不断增加样本量,扩大临床试验人数从而证明其有效性。”
就在两项在美临床试验结果揭晓当日,吉利德科学董事长兼首席执行官Daniel O’Day发布公开信表示,公司将在未来几周开放标签的3期SIMPLE试验的顶线结果。
Daniel O’Day还透露,在药物供应方面,目前供应量共计为150万剂,根据临床试验中正在研究的最佳治疗时间来计算,这一供应量可以满足超过14万个疗程的患者治疗。
据纽约时报和 CNN最新消息 ,FDA已经和吉利德就瑞德西韦展开沟通,将会尽快批准其作为COVID-19的新治疗方案。
此外,日本首相前几天也在会议上表示,若瑞德西韦在其他国家率先获批的话,日本也将积极推动该药物在本国的获批,最快将于5月做出决定。
